|
• Okładka • Program • Panele • Pokazy
|
XVII Festiwal Nauki w Warszawie (20-29.09.2013)
Wydział Farmaceutyczny Warszawskiego Uniwersytetu Medycznego
Spotkania weekendowe pokazy w laboratoriach i wykłady
|
|
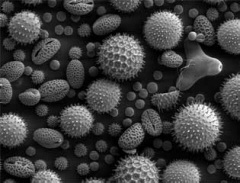
Pyłki kwiatowe
|
Wydział Farmaceutyczny WUM Banacha 1, Warszawa Sobota 21 września, godz. 11:00, 12:00 i 13:00 Wykład i prezentacja, limit każdorazowo 120 osób
Alergia wczoraj i dziś Dr Sławomir Białek 3
Najstarszym zapisem reakcji alergicznej jest opis śmierci faraona Menesa (XVII w. p.n.e.) - zmarł on nagle po użądleniu przez szerszenia. W talmudzie babilońskim znajduje się przepis na odpowiednie preparowanie białka jaj kurzych w przypadkach nadwrażliwości, a Hipokrates niezwykle dokładnie opisał duszność napadową, jak również pierwszy używał terminu "asthma" w odniesieniu do zaburzeń oddychania. Galen, nazywany ojcem farmacji, w II w.n.e. opisał objawy nadwrażliwości na zapach róż i na spożycie mleka. Jednak znaczący rozwój alergologii nastąpił dopiero w drugiej połowie XIX w. W 1839 r. F. Magendie opisał niewytłumaczalne w owym czasie zjawisko, a mianowicie wystąpienie gwałtownych objawów chorobowych po powtórnym wstrzyknięciu królikom tak nieszkodliwej substancji jak białko jaja kurzego. W 1873 r. Ch. Blackley związał przyczynowo gorączkę sienną z nadwrażliwością na pyłki roślin, a w r. 1906 C. von Pirquet wprowadził termin "alergia" w odniesieniu do sposobu reagowania odbiegającego od normy. Olbrzymi postęp w poznaniu mechanizmów reakcji alergicznych dokonał się po ustaleniu struktury chemicznej immunoglobulin. W 1968 roku dokonano klasyfikacji reakcji alergicznych, którą posługuje się dziś każdy badacz i klinicysta. Dzisiaj alergia, uczulenie lub nadwrażliwość, często klasyfikowana jako atopia, stanowi jeden z najbardziej powszechnych problemów zdrowotnych. Jest wywołana kontaktem pacjenta z substancjami zwanymi alergenami, które występują w otaczającym nas środowisku. Istnieje kilka typów alergii, różniących się mechanizmami odpowiedzi immunologicznej, a więc także szybkością pojawiania się objawów chorobowych. Objawy często występują po kontakcie z substancją, która dotychczas nie wywoływała zmian chorobowych. Pierwszy kontakt z alergenem powoduje powstanie reakcji pierwotnej, dzięki której organizm zasadniczo bezobjawowo "zapamiętuje" daną substancję na okres kilku dni lub nawet kilku lat. Po ponownym kontakcie z alergenem pojawia się właściwa reakcja uczuleniowa, wywołująca pełne objawy kliniczne choroby, którą nazywamy reakcją wtórną. Atopia jest dziedziczną odmianą alergii, a w przypadku jej występowania u jednego z rodziców prawdopodobieństwo zachorowania potomstwa wynosi 30%. Natomiast gdy obydwoje rodzice są alergikami, prawdopodobieństwo ujawnienia się atopii u dzieci wzrasta do 70%. Najwięcej zachorowań na alergię obserwuje się w krajach wysokorozwiniętych, w dużych aglomeracjach miejskich. W ostatnich latach nastąpił znaczny wzrost liczby przypadków schorzeń górnych dróg oddechowych (pyłkowica, całoroczny alergiczny nieżyt nosa), alergii pokarmowych i atopowej astmy oskrzelowej. W Polsce na alergię choruje około 30% populacji. Światowa Organizacja Zdrowia (WHO) zaliczyła choroby alergiczne do grupy chorób cywilizacyjnych, a na liście stwarzanych zagrożeń zostały one zaklasyfikowane na czwartej pozycji po nowotworach, chorobach układu krążenia i AIDS. Do głównych przyczyn gwałtownego wzrostu zachorowań na alergię należy zaliczyć powszechność szczepień ochronnych, terapie przy użyciu antybiotyków, podawanie witaminy D3, częste infekcje wirusowe, zmiany diety, zatrucie środowiska oraz tzw. "sterylność życia codziennego", która m. in. polega na dostępności uzdatnianej bieżącej wody w wodociągach, zastosowaniu kanalizacji i częstym używaniu środków higieny osobistej. Tematy spotkania: • Alergia - czym grozi? • Jakie substancje wywołują uczulenia i jak zapobiegać rozwinięciu się alergii? • Jak diagnozować i leczyć alergie? |
|
|
Wydział Farmaceutyczny WUM Banacha 1, Warszawa Sobota 21 września, godz. 11:00, 12:00 i 13:00 Pokaz, limit każdorazowo 10 osób Decyduje kolejność przyjścia
Nalewki owocowe kontra wolne rodniki (Dr A. Zielińska, dr K. Paradowska) 4
Wolne rodniki to bardzo reaktywne cząstki posiadające niesparowany elektron. W nadmiarze powodują one uszkodzenia biomolekuł, w tym DNA. Wiele prac wskazuje na związek między zmniejszoną odpornością na działanie rodników w komórkach a różnymi chorobami, np. rakiem, chorobami układu krążenia czy neurodegeneracyjnymi. Również w przypadku procesu starzenia wolne rodniki mają niejedno do powiedzenia. Jedną z najważniejszych grup rodników są rodniki tlenowe. Jeszcze kilkadziesiąt lat temu tlen był uważany za naszego największego sprzymierzeńca, bez którego życie na Ziemi nie rozwinęłoby się. Nikt nie przypuszczał, że niektóre jego formy mogą być czynnikiem niszczącym życie. Obecnie powstawaniu nadmiaru rodników sprzyja środowisko, w którym żyjemy – zanieczyszczenie powietrza, stres, nieodpowiednie odżywianie. Z wolnymi rodnikami możemy jednak walczyć. Antyoksydanty (przeciwutleniacze) neutralizują rodniki. W toku ewolucji organizmy żywe wytworzyły szereg mechanizmów obronnych, nie zawsze są one jednak wystarczające. Bardzo ważne jest więc uwzględnienie w diecie produktów bogatych w przeciwutleniacze takie jak witamina C i E, karotenoidy czy związki polifenolowe, jak flawonoidy, antocyjany czy taniny, znajdujące się głównie w owocach i warzywach. Jedną z postaci, w których mogą występować owoce jako składnik diety, są nalewki owocowe. Zapraszamy na pokaz do laboratorium, w trakcie którego wspólnie przeprowadzimy pomiary właściwości przeciwutleniających różnych rodzajów nalewek owocowych. Do tego celu wykorzystamy modelowy, barwny rodnik DPPH. Będzie można zbadać potencjał antyoksydacyjny niewielkiej liczby próbek własnych nalewek. Zapraszamy z próbkami!
Bibliogafia
|
|
|
Wydział Farmaceutyczny WUM Banacha 1, Warszawa Sobota 21 września, godz. 11:00, 12:00 i 13:00 Pokaz, limit każdorazowo 10 osób Decyduje kolejność przyjścia
Najwięcej C witaminy mają polskie owoce, warzywa, dziewczyny… (Dr Agnieszka Białek, K. Młodziejewska) 5
Witamina C (kwas L-askorbowy, lakton kwasu 2,3-dehydro-L-gulonowego) jest jedną z najmniej trwałych spośród witamin rozpuszczalnych w wodzie. Wykazuje silne właściwości redukcyjne i z tego faktu wynikają jej wszystkie funkcje biologiczne. Układ kwas L-askorbowy/kwas dehydroaskorbowy bierze udział w zachowaniu potencjału oksydoredukcyjnego w komórce i w transporcie elektronów. Jest stymulatorem licznych enzymów, biorących udział w procesach kluczowych dla funkcjonowania organizmu, np., w syntezie kolagenu, syntezie karnityny, katabolizmie tyroksyny, syntezie noradrenaliny. Zaburzenia w syntezie kolagenu są przyczyną szkorbutu (gnilca), który jest najbardziej znaną konsekwencją awitaminozy witaminy C. Witamina C poprzez udział w metabolizmie tkanki łącznej ma istotne znaczenie w procesie gojenia ran. Poprzez wpływ na biosyntezę karnityny kwas askorbowy ma pośrednio istotny wpływ na transport kwasów tłuszczowych do mitochondriów, a w konsekwencji na uzyskiwanie z nich energii. Ważne znaczenie ma również witamina C w procesach syntezy niektórych hormonów peptydowych (np. wazopresyny, oksytocyny czy melanotropiny) a także w detoksykacji organizmu, gdyż bierze udział w enzymatycznych przemianach ksenobiotyków w mikrosomach a także w wydalaniu jonów niektórych metali (kadmu, ołowiu, wanadu). Podkreśla się także znaczącą rolę kwasu askorbowego w profilaktyce choroby niedokrwiennej serca (poprzez zmniejszanie odkładania cholesterolu w ścianach naczyń krwionośnych) oraz jego zdolność do inaktywacji wielu reaktywnych form tlenu (rodnika tlenowego, rodnika hydroksylowego, tlenu singletowego). Witamina C ułatwia także wchłanianie żelaza (zwłaszcza niehemowego) z pożywienia. Głównym źródłem kwasu askorbowego dla człowieka są świeże i właściwie przetworzone owoce i warzywa. Ze względu na małą jej trwałość procesy technologiczne, takie jak np.: suszenie, solenie, parzenie, a także niektóre środki konserwujące (np. benzoesan sodu), powodują rozkład tej witaminy. Także enzymy z grupy oksydaz, obecne naturalnie w produktach spożywczych, a które ulegają uwolnieniu i aktywacji po uszkodzeniu lub zniszczeniu struktury tkankowej, np. podczas krojenia czy obierania, powodują rozkład witaminy C. Straty tej witaminy podczas przygotowywania potrawy mogą dochodzić nawet do 50%. Zawartość witaminy C w produktach spożywczych jest bardzo zróżnicowana. Podczas pokazu uczestnicy będą mieli możliwość przy pomocy nieskomplikowanych narzędzi analitycznych zbadać właściwości fizyko-chemiczne witaminy C oraz ocenić i porównać jego zawartość w różnorodnych produktach spożywczych oraz we własnym organizmie.
Bibliogafia:
|
|
Roślina transgeniczna |
Wydział Farmaceutyczny WUM Banacha 1, Warszawa Sobota 21 września, godz. 11:00, 12:00 i 13:00 Pokaz, limit każdorazowo 15 osób Decyduje kolejność przyjścia
Biotechnologia roślin leczniczych Dr Wojciech Szypuła 6
Naturalnym środowiskiem bytowania roślin, z którym stykamy się najczęściej, jest gleba. Obecnie istnieje jeszcze inna możliwość hodowli roślin - w warunkach sterylnych, przy zastosowaniu pożywki agarowej zamiast ziemi. W takim przypadku mówimy o hodowli in vitro, czyli w szkle. Metoda ta jest m. in. stosowana do szybkiego klonalnego mnożenia roślin, tj. otrzymywania wielu okazów potomnych z tkanki jednej rośliny. Istnieje także możliwość osobnego hodowania wyodrębnionych organów tkanek i komórek roślinnych, np. samych korzeni, zarodków lub komórek. Ponadto, zamiast roślin lub ich organów można również hodować niezróżnicowaną tkankę, nazywaną kalusem, lub prowadzić hodowlę komórek w zawiesinie w tzw. bioreaktorach. W tkankach wyhodowanych in vitro występują na ogół w podobnej ilości takie same związki biologicznie czynne, jak w roślinie macierzystej, co umożliwia otrzymanie ich z pominięciem hodowli całej rośliny. Najlepsze wyniki uzyskuje się z kultury zawiesinowej w bioreaktorach, w których parametry wzrostu są automatycznie rejestrowane i kontrolowane zewnętrznie na monitorze. Według jednej z najnowszych metod, związki lecznicze otrzymuje się z korzeni transgenicznych, tzn. mających wprowadzony obcy gen. Do modyfikacji genotypu używa się bakterii o nazwie Agrobacterium rhizogenes. Organizmy modyfikowane genetycznie (GMO - genetically modified organisms) otrzymywane są obecnie z bakterii, grzybów, roślin i zwierząt. Dostarczają one m.in. wielu produktów żywnościowych, obecnych na naszym rynku. Zasady postępowania regulowane są specjalnymi przepisami, według których na opakowaniu powinna być informacja, że artykuł pochodzi z roślin zmienionych genetycznie. Hodowla tkankowa roślin in vitro pozwala także otrzymywać rośliny haploidalne (z pojedynczym zespołem chromosomów), a także dokonywać fuzji protoplastów (nieobłonionych komórek) dwóch gatunków, nie dających mieszańców w stanie naturalnym. Tkanki można zamrażać i przechowywać w temperaturze ciekłego azotu (-196oC), a po powolnym rozmrożeniu kontynuować hodowlę. Można również otoczkować tkanki merystematyczne i przechowywać w stanie niezmienionym w niskiej temperaturze dodatniej w formie tzw. sztucznych nasion. Badania Katedry obejmują poszukiwania związków naturalnych o właściwościach cytostatycznych i immunomodulujących, które tworzą się w hodowli in vitro. Obecnie przedmiotem prac są różne gatunki cisa i inne rośliny nierosnące masowo w Polsce. Cis zawiera ok. 350 związków chemicznych, z których wiele jest trujących, natomiast jeden, paklitaksel, wykazuje właściwości przeciwnowotworowe. Związek ten powstaje również w hodowli in vitro. Jego obecność stwierdziliśmy w korzeniach transformowanych w ilości równej jego występowaniu w korze. Biotechnologia jest przedmiotem zajęć dydaktycznych i badań naukowych dwóch Katedr Wydziału Farmaceutycznego - Katedry i Zakładu Biologii i Botaniki Farmaceutycznej, która zajmuje się biotechnologią roślinną oraz Katedry i Zakładu Technologii Leków i Biotechnologii Farmaceutycznej, która zajmuje się biotechnologią mikroorganizmów i hodowlą grzybów. W trakcie pokazu zostaną zademonstrowane hodowle tkankowe w bioreaktorach oraz hodowle roślin transgenicznych. Nie zabraknie również czasu na dyskusję o uzyskiwaniu związków biologicznie czynnych z roślin. |
|
|
Afiliacje
3 Zakład Laboratoryjnej Diagnostyki Medycznej, Wydział Farmaceutyczny, Warszawski Uniwersytet Medyczny, ul. Banacha 1, 02-097 Warszawa, e-mail: slawomir.bialek@wum.edu.pl, tel./faks 22 5720 735, kierownik: prof. dr hab. Dariusz Sitkiewicz.
4 Zakład Chemii Fizycznej, Wydział Farmaceutyczny, Warszawski Uniwersytet Medyczny, ul. Banacha 1, 02-097 Warszawa, e-mail: agnieszka.zielinska1@wum.edu.pl, tel. 22 5720 950, kierownik prof. dr hab. Iwona Wawer.
5 Zakład Bromatologii, Wydział Farmaceutyczny, Warszawski Uniwersytet Medyczny, ul. Banacha 1, 02-097 Warszawa, e-mail: bromatologia@wum.edu.pl, tel./faks +22 5720 785, kierownik: prof. dr hab. Andrzej Tokarz
6 Katedra i Zakład Biologii i Botaniki Farmaceutycznej, Wydział Farmaceutyczny, Warszawski Uniwersytet Medyczny, ul. Banacha 1, 02-097 Warszawa, e-mail: wojciech.szypula@wum.edu.pl, tel./faks 22 5720 983, kierownik: prof. dr hab. Olga Olszowska.
|
|
|
O uczestnictwie decyduje kolejność rejestracji Pokazy przewidziane są dla gości indywidualnych ew. kilkuosobowych grup
|